Blood Direct PCR -kit
Funktioner
■ Enkelt och snabbt: PCR -amplifiering kan utföras direkt med hjälp av blod som mall, utan att de tråkiga stegen för provberedning och DNA -extraktion behövs.
■ Hög renhet: Hoppa över förbehandlingen av prov och DNA-extraktion kan hjälpa till att undvika korskontaminering av prover.
■ Hög genomströmning: PCR-identifiering för storskaliga prover kan utföras genom att kombinera satsen med 96/384-brunnars PCR-plattor.
■ Stark universalitet: Detta kit kan effektivt förstärka höga GC -fragment eller fragment med komplex sekundärstruktur och amplifieringslängden kan vara upp till 5 kb.
■ Stark motståndskraft mot spänning: Detta kit kan appliceras på olika arter och blodprover som bevarats på olika sätt.
Ansökningar
PCR-produkterna i detta kit innehåller "A" i 3'-änden, som kan användas direkt för TA-vektorkloning. Detta kit kan användas för amplifiering av genomiska DNA-fragment, genetisk analys med hög genomströmning och genotypning (t.ex. gendetektering).
Alla produkter kan anpassas för ODM/OEM. För detaljer,vänligen klicka på Anpassad tjänst (ODM/OEM)
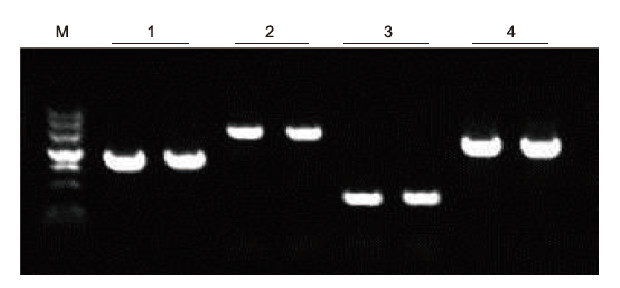 |
Med användning av human EDTA -antikoagulering som mall förstärktes 4 gener med olika GC -innehåll med Blood Direct PCR Kit. PCR -reaktionssystemet var 20 | il och 1 | il blod användes som mall. M: TIANGEN Marker II; 1: Fragmentstorlek 1090 bp, GC -innehåll 68,1%; 2: Fragmentstorlek 1915 bp, GC -innehåll 70,4%; 3: Fragmentstorlek 448 bp, GC -innehåll 74,8%; 4: Fragmentstorlek 1527 bp, GC -innehåll 61,5%. Experimentella resultat: Blood Direct PCR-kit kan effektivt amplifiera DNA-fragment med GC-innehållet i intervallet 61,5%-74,8%, vilket tyder på att det kan förstärka hög-GC-fragment. |
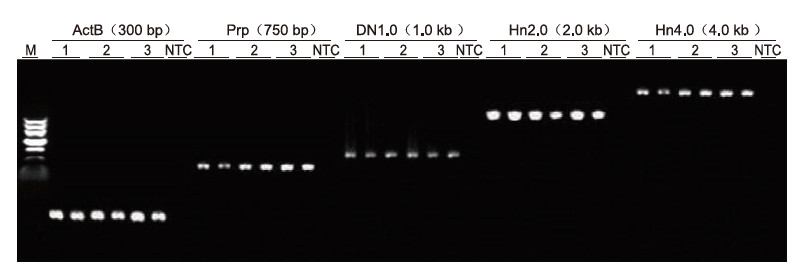 |
Med användning av human EDTA -antikoagulering som mall amplifierades 5 gener med olika längder (ActB, Prp, DN1.0, Hn2.0 och Hn4.0) med Blood Direct PCR Kit. PCR -reaktionssystemet var 20 | il och 1 | il blod användes som mall. M: TIANGEN Marker II; 1-3: 3 olika blodprov; NTC: kontroll utan primers. Experimentella resultat: Blood Direct PCR -kit kan förstärka fragment med en längd så lång som 4 kb, vilket tyder på att det kan förstärka långa fragment. |
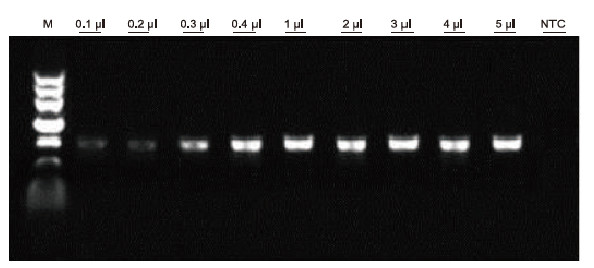 |
Med användning av human EDTA -antikoagulering som mall användes Blood Direct PCR -kit för PCR -detektion av olika blodprov. PCR -reaktionssystemet var 20 | il och 1 | il blod användes som mall. M: TIANGEN Marker II; 1-9: laddningsmängden blod är 0,1 μl, 0,2 μl, 0,3 μl, 0,4 μl, 1 μl, 2 μl, 3 μl, 4 μl respektive 5 μl; NTC: kontroll utan mall Experimentella resultat: Blood Direct PCR-kit har starkt motståndskraft mot blod och kan förstärka blodprover med lastningsintervallet 0,1-5 μl. |
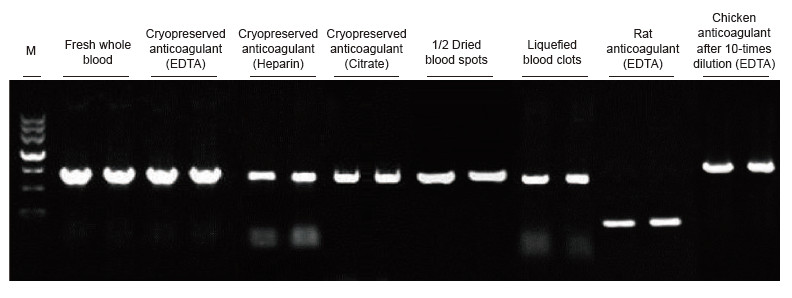 |
Blodprover från människa, råtta, kyckling och andra arter med olika behandlingar användes som mallar. Blood Direct PCR-kit användes för att amplifiera PRNP (human, 750 bp), Actin (råtta, 200 bp) och β-Actin (Chicken, 1,0 kb). PCR -reaktionssystemet var 20 | il och 1 | il blod användes som mall. M: TIANGEN Marker II. Experimentella resultat: Blood Direct PCR -kit kan appliceras på ett stort antal prover, och direkt PCR -detektion kan utföras på blodprov från olika arter med olika behandlingar. |
A-1 mall
■ Mallen innehåller proteinföroreningar eller Taq -hämmare etc. —— Rena DNA -mall, ta bort proteinföroreningar eller extrahera mall -DNA med reningskit.
■ Denatureringen av mallen är inte fullständig —— Lämpligt öka denatureringstemperaturen och förläng denatureringstiden.
■ Mallnedbrytning —— Förbered mallen igen.
A-2 Primer
■ Dålig kvalitet på primers —— Syntetisera primern igen.
■ Nedbrytning av primer —— Dela upp högkoncentrationsprimrarna i liten volym för bevarande. Undvik att frysa och tina flera gånger eller långvarig kryokonservering vid 4 ° C.
■ Felaktig design av primers (t.ex. primerlängd inte tillräcklig, dimer bildad mellan primers, etc.) -Design primers (undvik bildning av primer dimer och sekundär struktur)
A-3 mg2+koncentration
■ Mg2+ koncentrationen är för låg —— Rätt öka Mg2+ koncentration: Optimera Mg2+ koncentration genom en serie reaktioner från 1 mM till 3 mM med ett intervall på 0,5 mM för att bestämma den optimala Mg2+ koncentration för varje mall och primer.
A-4 Glödgningstemperatur
■ Den höga glödgningstemperaturen påverkar bindningen av primer och mall. —— Minska glödgningstemperaturen och optimera tillståndet med en lutning på 2 ° C.
A-5 Förlängningstid
■ Kort förlängningstid —— Öka förlängningstiden.
Fenomen: Negativa prover visar också målsekvensbanden.
A-1 kontaminering av PCR
■ Korsförorening av målsekvens eller förstärkningsprodukter —— Försiktigt att inte pipettera provet som innehåller målsekvensen i det negativa provet eller spill ut dem från centrifugröret. Reagensen eller utrustningen bör autoklaveras för att eliminera befintliga nukleinsyror, och förekomsten av kontaminering bör bestämmas genom negativa kontrollförsök.
■ Reagensförorening ——Allikvotera reagensen och förvara vid låg temperatur.
A-2 Primer
■ Mg2+ koncentrationen är för låg —— Rätt öka Mg2+ koncentration: Optimera Mg2+ koncentration genom en serie reaktioner från 1 mM till 3 mM med ett intervall på 0,5 mM för att bestämma den optimala Mg2+ koncentration för varje mall och primer.
■ Felaktig primerdesign och målsekvensen har homologi med icke-målsekvensen. —— Re-design primers.
Fenomen: PCR-förstärkningsbanden är oförenliga med den förväntade storleken, antingen stora eller små, eller ibland förekommer både specifika förstärkningsband och icke-specifika förstärkningsband.
A-1 Primer
■ Dålig primerspecificitet
—— Re-design primer.
■ Primerkoncentrationen är för hög —— Höj denatureringstemperaturen korrekt och förläng denatureringstiden.
A-2 mg2+ koncentration
■ Mg2+ koncentrationen är för hög ——Sänk korrekt Mg2+ -koncentrationen: Optimera Mg2+ koncentration genom en serie reaktioner från 1 mM till 3 mM med ett intervall på 0,5 mM för att bestämma den optimala Mg2+ koncentration för varje mall och primer.
A-3 termostabilt polymeras
■ Överdriven enzymmängd —— Minska enzymmängden på lämpligt sätt med intervallet 0,5 U.
A-4 Glödgningstemperatur
■ Glödgningstemperaturen är för låg —— Höj glödgningstemperaturen på lämpligt sätt eller använd tvåstegsglödgningsmetoden
A-5 PCR-cykler
■ För många PCR -cykler —— Minska antalet PCR -cykler.
A-1 Primer——Dålig specificitet ——Design primern, ändra primerns position och längd för att förbättra dess specificitet; eller utföra kapslad PCR.
A-2 Mall-DNA
——Mallen är inte ren —— Rena mallen eller extrahera DNA med reningssatser.
A-3 mg2+ koncentration
——Mg2+ koncentrationen är för hög —— Minska Mg korrekt2+ koncentration: Optimera Mg2+ koncentration genom en serie reaktioner från 1 mM till 3 mM med ett intervall på 0,5 mM för att bestämma den optimala Mg2+ koncentration för varje mall och primer.
A-4 dNTP
—— Koncentrationen av dNTP är för hög —— Minska koncentrationen av dNTP på lämpligt sätt
A-5 Glödgningstemperatur
—— För låg glödgningstemperatur —— Lämpligt öka glödgningstemperaturen
A-6 cykler
——För många cykler ——Optimera cykelnumret

Det första steget är att välja lämpligt polymeras. Vanligt Taq-polymeras kan inte korrekturläsas på grund av avsaknad av 3'-5'-exonukleasaktivitet, och felanpassning kommer att kraftigt minska förlängningseffektiviteten hos fragment. Därför kan vanligt Taq -polymeras inte effektivt amplifiera målfragment större än 5 kb. Taq -polymeras med speciell modifiering eller annat högfrekvent polymeras bör väljas för att förbättra förlängningseffektiviteten och uppfylla behoven för långfragmentförstärkning. Dessutom kräver amplifieringen av långa fragment också motsvarande justering av primerdesign, denatureringstid, förlängningstid, buffert-pH, etc. Vanligtvis kan primers med 18-24 bp leda till bättre utbyte. För att förhindra mallskador bör denatureringstiden vid 94 ° C reduceras till 30 sekunder eller mindre per cykel, och tiden för att stiga temperaturen till 94 ° C före förstärkning bör vara mindre än 1 min. Dessutom kan inställning av förlängningstemperaturen till cirka 68 ° C och utformning av förlängningstiden enligt hastigheten 1 kb/min säkerställa effektiv förstärkning av långa fragment.
Felhastigheten för PCR -amplifiering kan reduceras genom att använda olika DNA -polymeraser med hög trovärdighet. Bland alla Taq -DNA -polymeraser som hittills hittats har Pfu -enzymet lägsta felfrekvens och högsta trovärdighet (se bifogad tabell). Förutom enzymval kan forskare ytterligare minska PCR -mutationshastigheten genom att optimera reaktionsförhållandena, inklusive optimering av buffertkomposition, koncentration av termostabilt polymeras och optimering av PCR -cykelantal.
Produktkategorier
VARFÖR VÄLJA OSS
Sedan etableringen har vår fabrik utvecklat produkter i världsklass med principen
av kvalitet först. Våra produkter har fått ett utmärkt rykte i branschen och är värdefulla bland nya och gamla kunder.








